Задача
Качество является важной характеристикой любого продукта. Это сильнейшее конкурентное преимущество, которое укрепляет доверие клиентов и побуждает их возвращаться снова и снова.
Качество продукта определяется множеством свойств, но ключевым зачастую является одно. Для компьютера это производительность, для мебели - дизайн, для книги - то, насколько интересно читателю повествование. Для лекарственного препарата качество - это, в первую очередь, безопасность пациента.
С 2014 года в России введены в действие международные стандарты GMP (Good Manufacturing Practice, Надлежащие производственные практики), в основе которых лежат лучшие практики по организации работы фармацевтических производителей. Применение GMP позволяет гарантировать максимальную степень безопасности продукции за счет правильной организации процессов производства и контроля качества.

Но поддерживать высокое качество на протяжении всего жизненного цикла продукта нелегко. Почему?
GMP требует наличия регламентирующих документов по всем процессам, связанным с основной деятельностью фармпроизводителя. И это не только производство и лабораторный контроль, но и обучение персонала, работа с отклонениями, внедрение изменений, управление оборудованием, анализ рисков и еще несколько десятков различных направлений. В крупной компании это тысячи регламентов, процедур, методических инструкций, руководств, которые нужно постоянно поддерживать в актуальном состоянии.
Каждое действие, выполненное в соответствии с регламентирующим документом, должно быть запротоколировано. Это порождает огромное количество регистрирующих документов, которые подтверждают выполнение технологических операций, лабораторных исследований, прохождение обучения сотрудниками, расследование отклонений и т.п. Каждый созданный документ в обязательном порядке проверяется вторым лицом.
Все бизнес-процессы должны постоянно анализироваться на предмет повышения эффективности и их соблюдения всеми сотрудниками компании. Любой документ по требованию внешнего или внутреннего проверяющего должен быть быстро предоставлен для дальнейшего анализа.
С чем сталкивается директор по качеству при организации работы фармацевтической системы качества (ФСК) на основе бумажных документов?
- Недостаточная прозрачность работы. Отсутствие детальной информации о работе сотрудников в конкретный момент времени.
- Частичная потеря информации. Бумажный документ имеет ограниченные возможности накопления метаданных.
- Низкая скорость бизнес-процессов. Длительное перемещение бумаги между сотрудниками.
- Трудоемкость документирования. Создание, учет и передача адресату контролируемой копии может занимать до 30 мин.
И что, все так плохо с бумажными документами?
Конечно, нет. Привычная система управления качеством на бумаге имеет ряд плюсов.
- Понятные технологии. Все знают, как организовать процесс на бумаге.
- Устоявшаяся корпоративная культура. Пользователи привыкли и не всегда понимают, что работу можно улучшить.
- Минимальные капитальные вложения. Особенно на фоне операционных затрат.
Все больше и больше требований
С каждым годом контроль качества и требования к организации производства лекарств ужесточаются. В своем ежегодном послании Федеральному Собранию Владимир Путин заявил, что контроль качества лекарственных препаратов в РФ усилят на всех этапах. А это значит, что объем документооборота опять возрастет.
Можно ли будет реализовать ФСК на основе привычной «бумажной» системы документирования?
Да, можно.
С чем придется столкнуться фармацевтической компании при таком подходе?
- Необходимость дополнительных «рабочих рук».
- Ужесточение сроков.
- Больше отчетов.
- Двойной контроль.
Альтернатива есть!
На помощь приходит использование автоматизированных систем управления качеством (Electronic Quality Management System, eQMS). Многие западные компании уже пошли по этому пути.
Но на российском рынке наблюдается дефицит таких систем. Почему?
Дорого, санкции, мало кто хочет вкладываться в локализацию и маркетинг на неизвестном рынке.
Что делать?
Внедрять DirectumRX!
Акелон представляет решение по управлению Фармацевтической системой качества на платформе DirectumRX.

Наша цель – предоставить удобный инструмент и готовые модули для цифровой трансформации всех процессов фармацевтических производителей в единой, продуманной и технологичной среде.
Базовые принципы решения
- Все блоки фармацевтической системы качества в одном интерфейсе.
- Модульная структура.
- Полностью электронные документы и процессы.
- Автоматизация рутинных операций.
- Онлайн-мониторинг показателей.
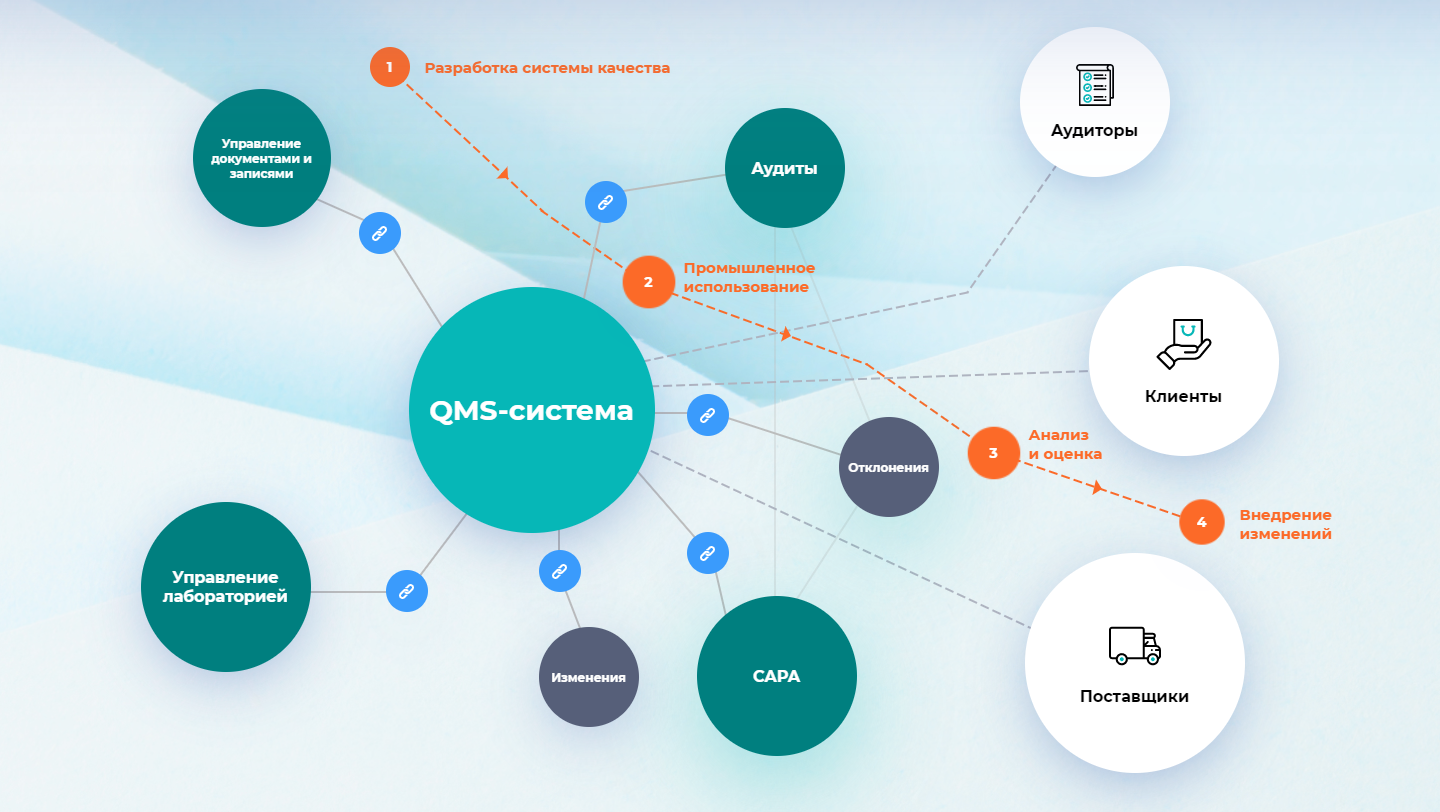
Автоматизация ФСК зачастую происходит поэтапно. На этапе выбора платформы важно понимать не только то, как система может автоматизировать наиболее актуальные процессы, но и то, что она может предложить в дальнейшем. Ключевым аспектом здесь является наличие готовых решений по всем разделам GMP. Ведь процессы документооборота, управления отклонениями, изменениями, CAPA, самоинспекциями, досье на серию и т.п. очень тесно переплетены между собой и используют сквозные данные. Их автоматизация в рамках одной платформы позволяет минимизировать затраты на инфраструктуру, интеграцию, внедрение и обучение пользователей при максимальной пользе для компании.
«Соблюдение фармацевтическими компаниями высоких стандартов GMP требует соблюдения высоких требований в стандартах разработки решений для этой отрасли. Только такая взаимосвязь позволит выпускать качественные продукты для здоровья миллионов людей. Я осознаю высокую ответственность, которая лежит на всех разработчиках решения и лично на мне», — Александр Волошин, разработчик технического решения по управлению ФСК.
Модули решения
Модуль предназначен для организации процесса управления отклонениями в соответствии с международным стандартом GMP.
Ключевые функции:
- Регистрация отклонений.
- Учет коррекций.
- Проведение расследования корневых причин.
- Подготовка данных для обзора по качеству.
Ключевой бизнес-эффект:
- Снижение сроков расследований отклонений
Модуль позволяет управлять корректирующими и предупреждающими действиями (CAPA) на всех стадиях — от формирования плана до оценки эффективности.
Ключевые функции:
- Разработка и согласование планов CAPA.
- Постановка и контроль выполнения действий.
- Планирование и анализ эффективности CAPA.
- Подготовка данных для обзора по качеству.
Ключевой бизнес-эффект:
- Ускорение процессов разработки, реализации и оценки эффективности CAPA.
Модуль предназначен для организации процесса управления изменениями в соответствии с международным стандартом GMP.
Ключевые функции:
- Ведение реестра изменений.
- Согласование плана изменения.
- Управление проектом внедрения изменения с использованием диаграммы Ганта.
- Подготовка данных для обзора по качеству.
Ключевой бизнес-эффект:
- Ускорение процессов внедрения изменений.
Модуль позволяет реализовывать деятельность по проведению самоинспекций от инициации и планирования до формирования и согласования отчетов по результатам проведения.
Ключевые функции:
- Ведение плана программ и аудитов.
- Учет квалификации аудиторов.
- Подготовка отчетов по аудиту, регистрация отклонений и изменений.
- Подготовка данных для обзора по качеству.
Ключевой бизнес-эффект:
- Снижение стоимости проведения самоинспекций.
Модуль предназначен для автоматизации проведения лабораторных испытаний.
Ключевые функции:
- Учет проб и образцов.
- Ведение электронных спецификаций исследований.
- Автоматизированное создания актов отбора проб, протоколов испытаний и аналитических листов
- Маршрутизация заданий на проведение лабораторных работ.
- Учет лабораторного оборудования.
Ключевой бизнес-эффект:
- Снижение стоимости подготовки комплекта лабораторной документации.
УПРАВЛЕНИЕ РЕГЛАМЕНТИРУЮЩЕЙ ДОКУМЕНТАЦИЕЙ ФСК
Модуль предназначен для организации полного цикла работы с регламентирующими документами — от планирования подготовки до вывода из обращения и архивирования.
Ключевые функции:
- Перевод документооборота в электронный вид.
- Работа с электронными формами и бланками.
- Электронное согласование и утверждение с помощью электронной подписи.
- Обучение сотрудников и учет компетенций по документам.
- Работа с контролируемыми и неконтролируемыми копиями.
Ключевой бизнес-эффект:
- Снижение стоимости работы с документами ФСК.
Ключевые результаты внедрение eQMS:
- Снижение сроков расследований отклонений.
- Ускорение процессов разработки, реализации и оценки эффективности CAPA.
- Ускорение процессов внедрения изменений.
- Снижение стоимости проведения самоинспекций.
- Снижение стоимости подготовки комплекта лабораторной документации.
- Снижение стоимости работы с документами ФСК.
Экспертное мнение
«Автоматизация Фармацевтической Системы качества (ФСК) является сегодня одним из очевидных путей ее совершенствования. Для того, чтобы обеспечить максимально эффективное функционирование ФСК, требуется хорошее информационное взаимодействие всех структурных подразделений предприятия. Добиться этого можно при наличии инструмента эффективно автоматизирующего функции Системы качества и объединяющем в единой среде имеющиеся в компании ресурсы и процессы», — Александр Степанов, заместитель генерального директора по качеству, АО ГЕНЕРИУМ.
Команда проекта
Команда разработчиков
Всех нас объединяет важная миссия:
Мы помогаем фармацевтическим компаниям внедрять технологии и инновации для обеспечения пациентов качественными, современными и доступными лекарственными средствами.
Планы развития
Сейчас мы ведем 3 проекта автоматизации системы качества в крупных российских фармацевтических компаниях. Скоро мы расскажем о них!
У вас похожая задача?
Обсудите реализацию с экспертом Directum

Авторизуйтесь, чтобы написать комментарий